Et de deux ! Après s’être penchée sur les noms de médicaments et avoir sonné le glas des marques ombrelles, l’Agence nationale de sécurité du médicament (ANSM) a publié dans la foulée de nouvelles recommandations destinées cette fois à normaliser l’étiquetage des emballages des médicaments sous forme orale solide (hors homéopathie). L’Agence a en effet constaté que, « si les mentions portées sur le conditionnement sont largement encadrées, leur disposition et leur typographie ne sont pas prédéfinies ». Avec ce texte, c’est désormais chose faite.
Trier, regrouper, aligner
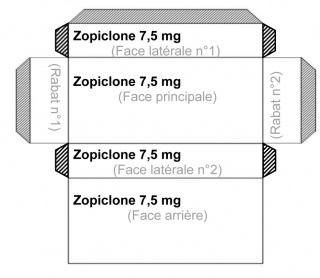
Le document, très technique et extrêmement détaillé, passe en revue tous les aspects liés à l’information disponible sur les emballages de médicaments : disposition et orientation des mentions, police d’écriture, couleur et matériaux, pictogrammes et logos ou encore espaces réservés au pharmacien. De manière générale, l’ANSM insiste sur le fait que « les mentions figurant sur un conditionnement doivent être facilement lisibles, clairement compréhensibles et indélébiles » et qu’il convient, par exemple, « de faire figurer dans un même champ de lecture les mentions correspondant à une idée commune afin qu’elles soient lues en même temps ». Pour les laboratoires, il faudra désormais grouper la ou les dénominations communes – qui devront « être mises en exergue » –, le dosage et la voie d’administration pour permettre une bonne identification du médicament. L’ANSM impose également des mentions présentes sur chaque face du conditionnement extérieur dans le sens de la longueur (voir schéma ci-dessus). L’ensemble du texte doit être orienté dans le même sens « afin de permettre la lecture […] selon un même axe de rotation ». Par ailleurs, « le choix des couleurs de l’étiquetage doit permettre d’améliorer la visibilité des mentions », prenant en compte les anomalies de la vision. L’étiquetage du conditionnement primaire des formes orales sous blisters, sachets, flacons ou tubes fait également l’objet de recommandations qui leur sont propres.